一、医疗器械不良事件监测工作进展
2020年,北京市医疗器械不良事件监测网络已覆盖到北京市医疗器械生产企业、一级以上医疗机构及主要医疗器械经营企业;国家医疗器械不良事件监测系统北京市有效注册用户达14440个,比2019年增加620个,其中经营企业用户为12067个,占用户总数的83.57%,器械注册人和备案人1313个(含进口产品代理企业),占用户总数的9.09%,医疗机构注册用户1060个,占用户总数的7.34%。
探索开展重点监测和再评价等上市后医疗器械安全性研究工作,完成了医用超声耦合剂再评价,提出了风险控制建议;完成了人工髋关节等6个品种的“十三五”重点监测工作,针对相关风险进行了深入研究,并提出风险控制建议。
二、可疑医疗器械不良事件报告情况
2020年,北京市监测单位上报的可疑医疗器械不良事件报告7118份,反映我市医疗器械报告意识良好;二级以上医疗机构连续七年消除零报告,注册人和备案人主动报告意识提升,各区报告覆盖率达到100%。
2020年,北京市共收到涉及北京市注册人和备案人的报告共计18211份,从医疗器械管理类别来看,Ⅰ类医疗器械相关报告1191例,占6.54%;Ⅱ类医疗器械相关报告10698例,占58.74%;Ⅲ类医疗器械相关报告6322例,占34.72%。(见附图)。Ⅱ类、Ⅲ类医疗器械的报告构成报告主体,与医疗器械风险程度高低相吻合。
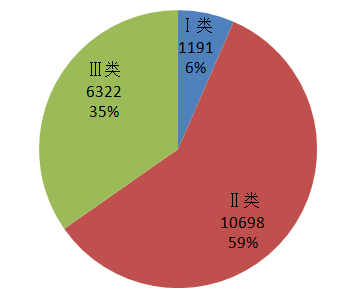
附图:涉及北京市注册人和备案人报告的器械管理类别分布
小贴士
1.北京市可疑医疗器械不良事件监测报告全部上报国家药品监督管理局,作为全国医疗器械不良事件监测数据,为全面评价器械风险,采取风险控制措施提供参考。
2.不同医疗器械的不良事件报告数量受使用数量、报告意识、风险程度等诸多因素影响。因此,各品种可疑医疗器械不良事件报告数的多少,不直接代表该医疗器械的不良事件发生率的高低,或实际风险程度的高低。
3.医疗器械不良事件定义:是指已上市的医疗器械,在正常使用情况下发生的,导致或者可能导致人体伤害的各种有害事件。
4.医疗器械不良事件监测定义:是指对医疗器械不良事件的收集、报告、调查、分析、评价和控制的过程。
5.医疗器械重点监测定义:是指为研究某一品种或者产品上市后风险情况、特征、严重程度、发生率等,主动开展的阶段性监测活动。
6.医疗器械再评价定义:是指对已注册或者备案、上市销售的医疗器械的安全性、有效性进行重新评价,并采取相应措施的过程。
来源:北京药品监督管理局